| Декалін і 1,4 диетилбензен |
| Східні хімічні властивості
|
ІІІ.

Зв'язок C-C є семіполярний, тому М=0, але дуже сильний + I
Етен,виявляючи позитивний індуктивний ефект, збільшує електронну густину бензольного ядра і поляризує його, тобто порушує в ньому рівномірний розподіл електронної густини. На вуглецевих атомах 2,4,6 виникає надлишок електронної густини
|

Декалін - дициклоалкан. Тому виявляє хімічні властивості циклоалканів.
|
| Сульфування
|
 |
 |
Нітрування:
 
Хлорування:
 
Окислення:
 
Відмінні хімічні властивості:
 
 
| 2-Хлорпентанол-1 і n-хлорфенол |

Зв'язок між атомом вуглецю і атомом хлору ковалентний. Але хлор більш електронегативний, ніж вуглець. Тому електронна пара зв'язку С→Cl значно зміщена до атому хлору, має заряд δ+
. Отже атом хлору виявляє -J.
Наявність у молекулі гідроксильної групи зумовлює кослотно-основні властивості. Оскільки атом кисню більш електронегативний, ніж атом вуглецю та водню, то електронна густина зміщується від цих атомів до кисню. Зв'язки О-Н і С-О поляризуються. В хімічних реакціях 2-хлоретанол-1 може віддавати протон, виявляти таким чином кислотні властивості. Тому у спиртів іде розрив С-О і О-Н зв'язків.
Крім того на атомі кисню гідроксильної групи спирту є вільні пари електронів. За рахунок цих електронів 2-хлоретанол-1 може також приєднувати протон до атому кисню ОН-групи і виявляти при цьому основні властивості. Отже 2-хлоретанол-1 виявляє кислотно-основні властивості
|

+ М ефект виявляють атоми і групи атомів, які мають вільні електронні пари.
Зв'язок С-О скорочується і зменшується, зв'язок О-Н додатково поляризується. Це приводить до того, що Н+
швидко відщеплюється у вигляді протону.
Електронно-акцепторні замісники збільшують кислотні властивості фенолів. Cl-замісник І-роду, електронно-акцепторний замісник.
У фенолів відбувається розрив О-Н зв'язків У фенолів більші кислотні властивості, ніж у спиртів.
|
2-Хлоретанол-1 і n-хлорфенол
Мають гідроксильну групу і атом галогену.
Цим обумовлені їх східні властивості. 1. Взаємодія з Ме
 
| Реакція гідроксильної групи |
| 1. Реакція з галогеноводнями |
2-хлорпентанол легко реагує з галогеноводнями і утворює при цьому алкілгалогеніди.

|
 |
| 2. Взаємодія з галогенідами фосфору або тіонілхлоридом |


При взаємодії РС13
з первинними спиртами як побічний продукт утворюється складний ефір фосфористої кислоти:


|



|
| Заміщення гідроксилу на аміногрупу |


|


|
| Реакція з розривом О-Н зв'язку |
| Це реакція етерифікації |
Спирти реагують з мінеральними і органічними кислотами

|
Феноли з карбоновими кислотами естерів не утворюють, а утворюють естери з ангідридами і галогенагідридами карбонових кислот

|
| Дегідратація |
При нагріванні спиртів в присутності Н2
SO4
або H3
PO4
або Al2
O3
відбувається вилучення води та утворюється подвійний зв'язок. Це внутрішньомолекулярна дегідратація


|
Феноли в реакції дегідрації не вступають, але здатні утворювати етери за умов реакції Вільсона

|
| Реакції окислення |
 |
 |
| Сульфування |
 |
 |
| Відмінні хімічні властивості |
Дегідрування
Реакція з водою є оборотною

При дії на 2-хлоретанол-1 водного розчину лугу, води або вологого оксиду срібла утворюють спирти:

Взаємодією 2-хлоретанол-1 з солями синильної кислоти добувають ціанисті алкіли (нітрили) та ізоціаміди (ізонітрили).

Реакція з солями срібла

Дегідрогалогенування

Взаємодія з Ме

Взаємодія з металічним Mg

Реакція з галогеноводнями

Реакція етерифікації.2-хлоретанол вступає в реакцію з мінеральними і органічними кислотами. Продуктами такої взаємодії є відповідні складні ефіри.

|
Галогенування


Нітрування

Перегрерупування Фріса

Нітрозування

Реакція Рейлера Тімана

Гідроксіметалювання
Це взаємодія фенолів з формальдегідами


|
| Бензосульфохлорид і бензоїлхлорид |
 |
 |
Збільшення електронної густини відбувається в бік атому О.
АтомSмає недостачу (дефіцит) електронів. Тобто несе δ+ заряд.
Тому зміщення π-електронної густини відбувається в бік S атома.
|
Збільшення електронної густини відбувається в бік атому О.
АтомСмає недостачу (дефіцит) електронів. Тобто несе δ+ заряд.
Тому зміщення π-електронної густини відбувається в атому бік S.
Найхарактернішими є реакції заміщення галогену (S-реакції). Висока полярність зв'язків С-Сl зумовлює високу реакційну здатність.
|
Східні хімічні властивості обумовлені наявністю бензольного кільця
Для ароматичних сполук властиві реакції електрофільного заміщення
|
| 1. Реакція галогенування |
 |
 |
| 2. Нітрування |
 |
 |
| 3. Сульфування |
 |
 |
| 4. Реакції приєднання |

|
 |
| 5. Гідроліз |
 |
 |
| Відмінні хімічні властивості |


Взаємодіє з водним розчином NH3
або (NH4
) 2
CO3
у присутності NaOH, NaHCO3
або інші з утворенням бензолсульфамідів, наприклад:
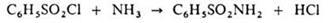
Взаємодіє зі спиртами

Реакція з нуклеофільними реагентами приводить до продуктів заміщення атома Сl.

При приєднанні С до ацетиленів у присутності солей Сu утворюються ненасичені α-хлорсульфони; при відновленні металами в нейтральному середовищу солі сульфінових кислот; у кислому середовищі або під дією LiAl4
-тіоли; з ароматичними сполуками в умовах реакції Фриделя-Крафтса-сульфони або, якщо при відриві SO2
утвориться стабільний карбокатіон, продукти алкілірування

|
О-ацилювання

N-ацилювання

C-ацилювання


Бензоїлуванням фенолу за реакцією Шоттен - Баумана добувають феніловий ефір бензойної кислоти:

Гідроксіметалювання
Це взаємодія фенолів з формальдегідами

|
Список использованной литературы
1. В.М. Домбровський, В.М. Найдан Органічна хімія; Київ, Вища школа, 1992.
2. Ф. Кери, Р. Сандберг Углублённый курс органической химии; Перевод с английского, Москва "Химия", 1981.
3. Дж. Робертс, М. Касерио Основы органической химии, перевод с английского, Издательство "Мир", Москва, 1978.
4. Избранные главы из курса "Органическая химия", Пособие для студентов. Новосибирск, 1999.
5. http: // www. cleopatra. ru/cosmetology/
|